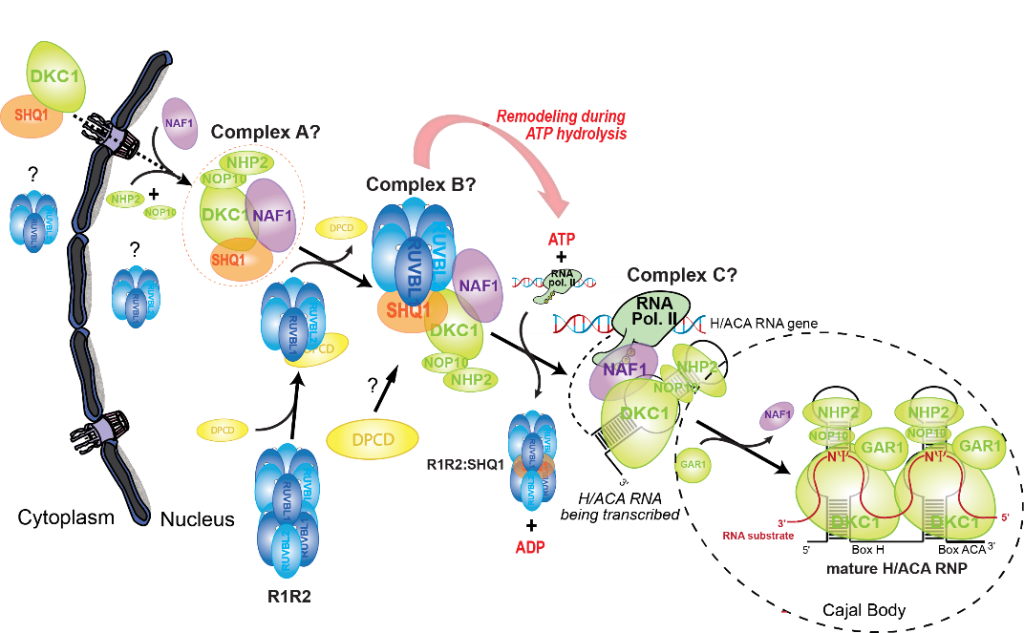
Core proteins are in green and assembly factors are in purple (NAF1), orange (SHQ1), blue (R1R2), and yellow (DPCD). The red and black hatched circles represent the intermediate complex isolated in cellulo
ANR HACA
Durée : 2026-2030
Montant : 530 000 €
Financeur : ANR
Coordinateur : Xavier Manival
Equipe(s) IMoPA : RNA/P
Projet HACA
Deciphering the early steps in the H/ACA snoRNP assembly
This project is devoted to the study of the biogenesis of the H/ACA RNPs, that contain one H/ACA RNA associated with two hetero-tetramers of GAR1, NHP2, NOP10, and DKC1 proteins. Various classes of H/ACA RNPs are involved in several crucial processes in cells. H/ACA RNP biogenesis requires chaperones and co-factors to promote assembly, and tertiary and quaternary folding: the R2TP complex, SHQ1, NAF1, and DPCD. R2TP is a generalist assembly platform that chaperones macromolecular complexes. Its function in H/ACA RNP assembly is still unclear. Given the large repertoire of box H/ACA RNPs with multiple crucial functions in cells and that defects in their biogenesis are linked to multiple diseases, it is essential to understand how this assembly is catalyzed and regulated. On the basis of our preliminary data, we propose that several protein-only intermediate complexes are formed successively during the early stages of H/ACA RNP assembly before association with the H/ACA RNAs. We will address the following questions: 1) What are the protein-only pre-complexes successively formed before the interaction of the core proteins with H/ACA RNA? What are their compositions, stoichiometries, and 3D structures? 2) What is the function of the R2TP in SHQ1 recruitment/release, and the importance of its ATPase activity? 3) What are the molecular determinants of R2TP specificity towards H/ACA RNP assembly, and especially what is the function of DPCD in this process? To achieve this, we will use cutting-edge techniques: (i) in vivo IP purification of cellular macro-complexes, (ii) reconstitution of pre-complexes by co-expression in vitro, (iii) nMS and MP for their characterization, and (iv) single-particle cryo-EM for their 3D structure resolution.
PARTENAIRES
- Lab of Sarah Cianferani, University of Strasbourg, Strasbourg
- Lab of Tiago Bandeiras, iBET, Oeiras, Portugal
Multinucleated osteoclast and its actin filament network. Fluorescence microscopy image from HAL-03356534v1.
ANR DynamOC
Durée : 2025-2028
Montant : 846 834 €
Financeur : ANR
Coordinateur : Claudine BLIN
Equipe(s) IMoPA : CImIND
Projet DynamOC
Understanding the dynamics of osteoclasts in growth and ageing
Osteoclasts (OCLs) are multinucleated myeloid cells responsible for bone resorption throughout life. Their function and proportion change with age, and their mode of resorption varies according to gender. But little is known about how these changes are controlled by age- and sex-dependent environmental modifications, and whether the same or different populations of OCLs are involved in these various conditions. As myeloid cells, OCLs are characterized by their diversity, made more complex by their ability to fuse with different progenitors and mature myeloid cells. Our consortium has demonstrated in adult female mice the existence of several populations of OCLs with distinct properties. But it is not known whether different or identical fusion partners contribute to each OCL population, and whether they change with age and sex.
Our objectives are to explore the diversity of OCLs as a function of age and sex in mice, to understand how the different populations of OCLs evolve in association with the bone marrow environment. We will validate our results on bone samples from men and women of different ages. Our consortium brings together experts in OCL biology, osteoimmunology, myeloid cell diversity, cell fusion and bone pathophysiology. By combining state-of-the-art transcriptomic and imaging technologies with in vitro and in vivo assays, we will explore the phenotypic and functional properties of OCLs and their dynamics of fusion. This project offers an original vision of OCL dynamics across age and gender. It will provide highly innovative information that will also help us to understand how these changes contribute to the development of OCL-related pathologies.
PARTENAIRES
- Claudine BLIN, LP2M (Coordinator), Nice
- Christel VEROLLET, IPBS, Toulouse
ANR ATCHOUM
Durée : 2025-2028
Montant : 687 000 €
Financeur : ANR
Coordinateur : Hervé Kempf
Equipe(s) IMoPA : CARPATH
Projet ATCHOUM
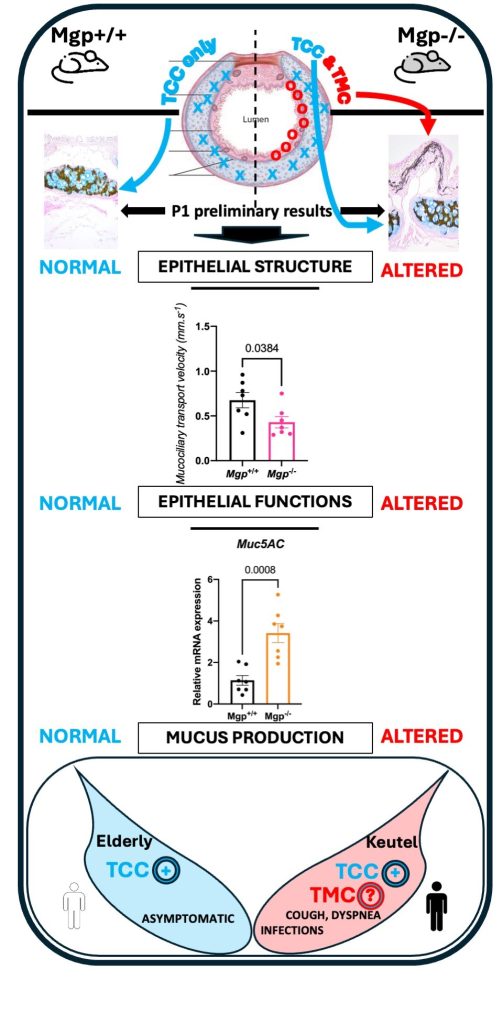
Abnormal Tracheal Calcification: Highlighting Overlooked and Unexplored Mechanisms
The trachea is a vital airway lined by a mucosal layer that clears inhaled pathogens, while cartilage rings provide structural support. In respiratory diseases, these defenses weaken, leading to excess mucus, inflammation, impaired clearance, increased infection risk, and airway collapse—features also observed in tracheal calcification (TC), a condition marked by abnormal calcium deposits that often go unnoticed clinically. TC is mainly detected in elderly patients or in those receiving long-term anti-vitamin K therapy, and is a hallmark of Keutel syndrome (KS), caused by mutations in Matrix Gla Protein (MGP), a key inhibitor of soft-tissue calcification. Excessive calcification of tracheal cartilage rings has been thought to drive respiratory symptoms. However, recent findings in Mgp-deficient mice reveal not only early tracheal cartilage calcification (TCC) but also a newly identified mucosal calcification (TMC) associated with epithelial alterations. These observations suggest that TMC may play a central role in respiratory dysfunction. The ATCHOUM project will investigate the contribution of TMC to airway decline in KS and other calcifying disorders, challenging the current view that symptoms arise solely from cartilage stiffening.
PARTENAIRES
- Institut Mondor de Recherche Biomédicale (Créteil)
- Université de Poitiers (Poitiers)
- Institut Imagine (Paris)
- CHU de Nice (Nice)

ANR StemIBD
Durée : 2024-2027
Montant : 775 526 €
Financeur : ANR
Coordinateur : Abdelilah WAKKACH
Equipe(s) IMoPA : CImIND, IHU INFINY, David MOULIN
Projet StemIBD
Origin and function of stem-like Th17 cells in chronic inflammatory bowel disease
Inflammatory bowel disease (IBD) is characterized by severe gut inflammation associated with various extra-intestinal inflammatory manifestations, affecting up to 50% of patients and causing even greater morbidity than the intestinal disease itself. Inflammatory CD4+ T cells, particularly Th17 cells, play an important role in this pathology, and at the same time these cells are essential for the integrity of the epithelial barrier and host defense against infection. However, the origin of this dichotomy within Th17 cells remains unclear. In several mouse models of colitis, our preliminary results showed that these Th17 cells are indeed heterogeneous. They contain several subsets including effector cells and a pool of stem-like cells. Interestingly, our preliminary results suggest that this pool of stem-like cells may constitute a reservoir from which pathogenic T cells can differentiate and contribute to IBD. Our overall aim is to decipher the cellular and molecular mechanisms that control the generation of the stem-like pool and the factors that influence their program of differentiation into inflammatory T cells. The originality of this project is the combination of murine models and patient biopsies in order to address the unresolved mechanisms that control the origin and maintenance of Th17 stem-like cells, as well as their differentiation and contribution to IBD. Our results will help to improve and/or propose new therapeutic strategies for IBD and associated extra-intestinal inflammatory manifestations.
PARTENAIRES
- Abdelilah WAKKACH, LP2M (Coordinator), Nice
- Julien MARIE, CRCL, Lyon

FEDER DREAM
Durée : 2024-2028
Montant total de l’aide européenne : 2 485 965 €
Coordinateur : JP PEHL
Projet FEDER DREAM 2024 – 2028
Dispositifs de REparation et d’Assistance Médicale
CONTEXTE
Dans ce projet, nous souhaitons étudier les tissus natifs ainsi que les matériaux de substitution utilisés pour recréer, réparer ou assister les tissus et organes atteints. En particulier, nous nous intéresserons à certains aspects de la réparation (ou assistance) d’un tissu ou d’un organe au niveau des membres supérieurs et inférieurs (orthopédie, réadaptation et rééducation), crâniofacial (oto-rhino-laryngologie, chirurgies maxillo-faciale et orale), du thorax (cardiologie et chirurgie thoracique) et de la reconstruction (chirurgie plastique réparatrice). Indépendamment de la spécialité étudiée, les tissus peuvent être regroupés en 3 grandes catégories, en fonction de leurs propriétés mécaniques et physiques : les tissus mous, les tissus durs et les tissus intermédiaires. Nous caractériserons les propriétés i) des muscles (squelettique, cardiaque) et de la muqueuse pour les tissus mous, ii) des os pour les tissus durs et iii) des cartilages et tissus calcifiés pour les tissus intermédiaires. Ainsi, le projet Dispositifs de REparation et d’Assistance Médicale (DREAM) a pour finalité i) de développer des prothèses, orthèses ou membranes innovantes et bio-inspirées, destinées à différentes spécialités médicales et également ii) d’améliorer les dispositifs médicaux déjà existants d’un point de vue durabilité et fonctionnalité. Ce projet pluri- et transdisciplinaire innovant de recherche, de développement, de valorisation et de transfert industriel est basé sur l’ingénierie tissulaire pour la médecine personnalisée permettant de réparer et/ou de réduire des séquelles liées aux pathologies temporaires ou permanentes.
L’objectif final vise à réduire les séquelles fonctionnelles, esthétiques et sociales et accélérer le transfert vers l’industrie biomédicale en développant une production locale à coûts raisonnés.
AXES DE RECHERCHE
1. Orthopédie, réadaptation et rééducation
Médecine régénératrice du cartilage (bio-impression 3D de cartilage de substitution).
Prothèses et orthèses personnalisées, ergonomiques et connectées. Suivi médical et numérique via jumeaux virtuels.
2. Chirurgie crâniofaciale, maxillofaciale, orale, plastique et réparatrice
Reconstruction ou la régénération des tissus osseux, muqueux et cartilagineux, essentiels aux fonctions vitales (respiration, alimentation, goût, odorat) et à l’esthétique faciale.
3. Cardiologie et chirurgie thoracique
Trachée : matériaux de substitution suturables, capables d’induire la régénération muqueuse respiratoire. Applications cardiovasculaires : Développement d’une membrane conductrice en polymère organique permettant un suivi cardiaque 12 dérivations simple. Surveillance de l’arythmie cardiaque et suivi personnalisé via IA. Application spécifique aux porteurs de prothèses de membres inférieurs pour évaluer effort et fatigue.
L’équipe ReMPaCOAT d’IMoPA (Astrid PINZANO DR CNRS // Laurent GROSSIN CRCN CNRS) est plus spécifiquement impliquée dans l’axe de recherche intitulé « Orthopédie, réadaptation et rééducation » où les compétences de l’équipe en médecine régénérative à visée ostéo-articulaire sont sollicitées.
Les objectifs DREAM dans la chirurgie régénératrice orthopédique auront pour but de combler la perte de substance dans la zone lésée du cartilage afin de favoriser la régénération tissulaire et le maintien de la fonction tissulaire. Ceci permettra d’ouvrir des perspectives thérapeutiques dans le cadre des greffes de substituts cartilagineux dans des modèles in vivo de lésions du cartilage. Ce cartilage de substitution produit in vitro pourra également servir d’outils de choix pour l’évaluation de nouvelles stratégies thérapeutiques ou substances pharmacologiques afin de limiter le recours à l’expérimentation animale.
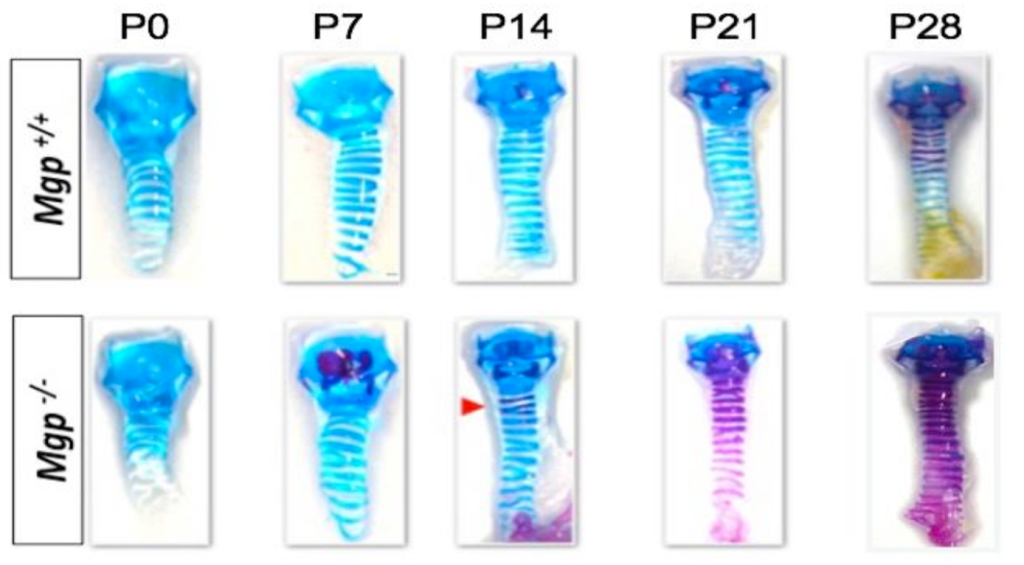
Whole-mount Alcian Blue (cartilage) and Alizarin Red (mineralization) stainings in P0, P7, P14, P21 and P28 trachea from Mgp+/+and Mgp-/- mice. This demonstrates that calcification of the trachea starts in the upper rings at P14 in Mgp-/- mice and spreads rapidly in the whole trachea at P21 and P28, whereas it only initiates at P28 in Mgp+/+
TRACHEO-TOMIC
Durée : 2025-2026
Montant : 11 000 €
Financeur : Fondation Maladies Rares ; AAP Genomics
Coordinateur : Hervé Kempf
Equipe IMoPA : CARPATH
TRACHEO-TOMIC
Identification of pathogenic pathways responsible for abnormal tracheal calcification in a mouse model of Keutel Syndrome
Although tracheal calcification (TC), a process observed during aging and in several diseases, can lead to significant respiratory complications, the underlying cellular and molecular mechanisms remain poorly understood and largely unexplored experimentally. Using detailed postnatal histological analyses in mouse trachea, we recently demonstrated that TC is (i) an early and abrupt event, (ii) progresses in a rostro-caudal manner, (iii) is tightly regulated over time, and (iv) is markedly accelerated in the absence of Matrix Gla Protein (MGP). These unexpected findings establish a robust and reproducible mouse model that enables deeper mechanistic investigations. Building on this exploratory work, our project will perform the first transcriptomic analysis of the dynamic progression of TC in wild-type and Mgp-deficient mice, in collaboration with the GenomEast platform in Strasbourg. We anticipate uncovering, for the first time, the key signaling pathways and transcriptional signatures driving TC during postnatal development.
PARTENAIRES
Prestation par la Plateforme GenomEast (Strasbourg)
ANR BioRiboSRP
Durée : 2021-2026
Montant : 508 000 €
Financeur : ANR
Coordinatrice : Séverine Massenet
Equipe(s) IMoPA : RNA/P
Projet BioRiboSRP
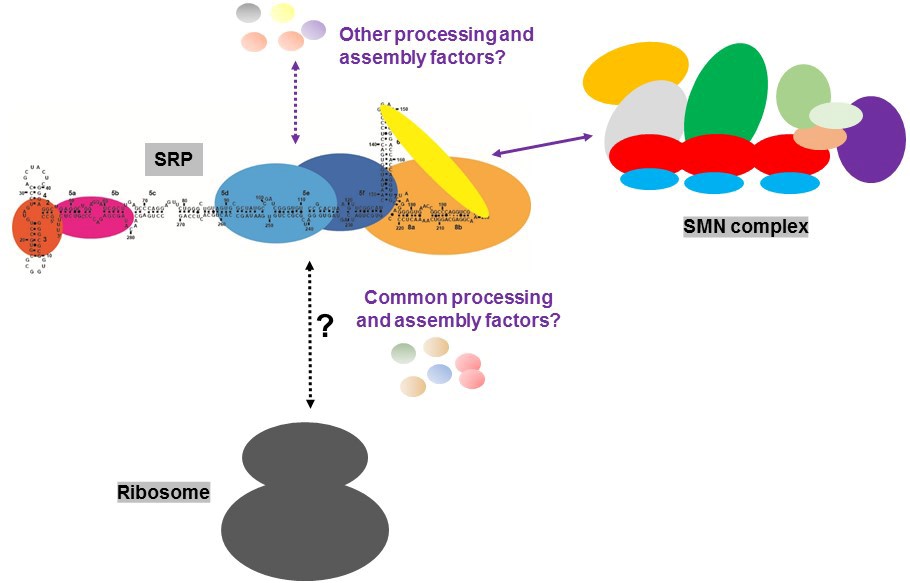
Deciphering the biogenesis of the Signal Recognition Particle, and its connections with ribosome biogenesis and nucleolar structure.
Many cellular functions are achieved by a family of molecular machines made of RNA-protein complexes, called non-coding ribonucleoprotein particles (ncRNP). Many factors are dedicated to the biogenesis of ncRNPs. These factors chaperone free subunits, increase the specificity of assembly, control the quality of the particles produced, etc, … How ncRNP assembly is catalyzed and regulated is still poorly understood. This project is dedicated to the study of the biogenesis of the universally conserved Signal Recognition Particle (SRP), which is essential for targeting transmembrane and secretory proteins to the endoplasmic reticulum. SRP assembly takes place mainly in the nucleolus where most of the SRP proteins associate with the 7SL RNA, while SRP54 association occurs later in the cytoplasm. In this project, we will identify the pathway of SRP biogenesis and the trans-acting factors involved, using several complementary unbiased high-throughput approaches, including 1) quantitative proteomics to identify the SRP subcomplexes and assembly intermediates, as well as the proteins associated with each of the SRP proteins; and 2) large-scale screens with visual readouts to detect proteins whose absence leads to defects in SRP biogenesis. We will examine functionally in detail the most promising factors identified in our screens, using a battery of in cellulo and in vitro approaches. We will identify assembly intermediates by expressing mutants of SRP proteins or depleting one of the SRP proteins.
PARTENAIRES
- Lab of Denis Lafontaine, Brussels, Belgium
- Team of Céline Verheggen, IGH, Montpellier

FEDER-REACT-EU
Durée : 2021-2023
Montant total de l’aide européenne : 1 780 582 €
Coordinateur : Xavier Manival
Projet MolAI4Cryo
Modeling and Artificial Intelligence for Cryo-EM 3D structures to fight COVID
MolAI4Cryo a pour objectif de décrypter l’interaction entre les protéines du coronavirus et la machinerie d’épissage des ARN messagers cellulaires de l’hôte afin de proposer de nouvelles cibles antivirales à finalité thérapeutique pour lutter contre la COVID-19. Ce projet nous permettra également d’améliorer notre connaissance sur les mécanismes d’infection virale de la cellule et de ces impacts à plus long terme.
La conduite de ce projet a nécessité la mise en place d’une plateforme de Cryo-microscopie, avec l’achat, entre autre, d’un Microscope Glacios 2 et d’un Vitrobot.
PARTENAIRES
IMoPA
UAR 2008 IBSLor


FEDER-FSE Lorraine et Massif des Vosges 2014-20
Durée : 2014-2020
Montant total de l’aide européenne : 298 500 €
Coordinateur : David Moulin
Projet TARGET
Translational research in Articular and Gastrointestinal inflammatory diseases in Grand-EsT
En 2014, le FEDER a accordé une subvention de 298 500 € au projet TARGET Translational research in Articular and Gastrointestinal inflammatory diseases in Grand-EsT. Ce projet est cofinancé par l’Union Européenne dans le cadre du Programme opérationnel FEDER-FSE Lorraine et Massif des Vosges 2014-2020.
L’ objectif de ce projet est l’identification de signatures moléculaires/cellulaires traduisant les mécanismes physiopathologiques des maladies inflammatoires chroniques intestinales (MICI), et des rhumatismes inflammatoires chroniques (RIC), et/ou d’évaluer la sensibilité ou la non-réponse aux biothérapies.
La conduite de ce projet a nécessité l’acquisition d’un cytomètre conventionnel de pointe : le BD FACSymphony A3. C’est un outil analytique puissant qui permet à ses utilisateurs d’identifier et d’analyser des phénotypes distinctifs dans des populations hétérogènes. Il utilise pleinement les progrès de l’instrumentation, du développement de fluorochrome et de la bio-informatique. Doté de 5 lasers avec 28 paramètres couleurs, il est dédié à des études multi-paramétriques complexes.
Système le plus sensible et rapide du marché, il permet à ses utilisateurs la recherche d’évènements rares. La configuration de l’équipement permet d’utiliser différentes longueurs d’ondes et des puissances traditionnelles et/ou uniques.
Ses spécificités :
Les performances de diffusion sont optimisées pour la résolution des lymphocytes, des monocytes et des granulocytes.
Il offre la possibilité d’analyser tout un ensemble de phénotypes et d’interroger, de manière très précise, des sous-ensembles cellulaires.
Sa résolution élevée permet la séparation des plaquettes fixées ; des billes de 0,3 μm ; des billes fluorescentes de 0,1 μm du bruit électronique.







